規制の概要
医薬品包装材料の定義と分類
中国薬局方によると、医薬品包装材料とは、医薬品メーカーが製造した医薬品や医療機関が調製した製剤と直接接触して使用される包装材料および容器を指します。 また、医薬品に直接接触しないが、医薬品に作用する医薬品包装材料(例えば、医薬品に直接接触せず、酸素・水バリア効果を有するアルミプラスチック包装材)も、医薬品包装材料として登録・監督する必要があります。
医薬品包装材料は通常、高リスクと非高リスクの2つのカテゴリに分類され、そのうち高リスクの医薬品包装材料には一般的に次のものが含まれます。
吸入製剤、注射剤、眼科用製剤の医薬品包装材料。
国家薬品監督管理局が監視データに従って監督することを特に要求する医薬品包装材料。
中国における医薬品包装材料の規制基準とモデル
中国薬局方は、国家医薬品標準システムの重要な部分として、中華人民共和国の公布された医薬品管理法、中華人民共和国の医薬品管理法の実施規則、医薬品包装材料の登録材料の要件、およびさまざまな技術ガイドラインおよび通知とともに、国家医薬品包装材料規格(YBB規格と呼ばれる)とともに、医薬品包装材料の監督のための規制システムが構成されています。 国家薬品監督管理局の公告(告示第56号[2019])によると、中国における医薬品包装材料の監督は、以前の登録管理システムから登録システムに移行し、技術審査は医薬品製剤または原薬に関連して実施され、承認審査がより効率的で科学的になりました。
 中国における医薬品包装資材の規制
中国における医薬品包装資材の規制
規制当局とその責任

国家薬品監督管理局(NMPA)は、国家市場監督管理総局(SAMR)の一部であり、以下の業務を担当しています。
· 各省の監督検査の状況と必要性に応じて、関連する検査基準を適時に改訂しなければならない。
必要に応じて、API、医薬品賦形剤、医薬品包装材料の現地検査および検査を組織します。

医薬品評価センター(CDE)はNMPAの一部であり、次のことを担当しています。
· API、医薬品賦形剤、医薬品包装材料の登録プラットフォームとデータベースを確立する。
· API、医薬品賦形剤、医薬品包装材料の登録データの受領、完全性、付与、公開、ならびにAPI、医薬品賦形剤、医薬品包装材料、医薬品製剤の審査および承認。

省の医薬品管理局はNMPAに従属し、地元の医薬品包装材料メーカーを監督しています。 地方局の主な責任は次のとおりです。
· 行政区域内のAPI、医薬品賦形剤、医薬品包装材料の日常的な生産企業を監督および管理します。
· 登録情報に基づく医薬品包装材料サプライヤーの監督と検査を強化し、法令に従って品質問題のある製品をタイムリーに調査および処理し、市販製品の評価と廃棄を行います。
登録プロセス
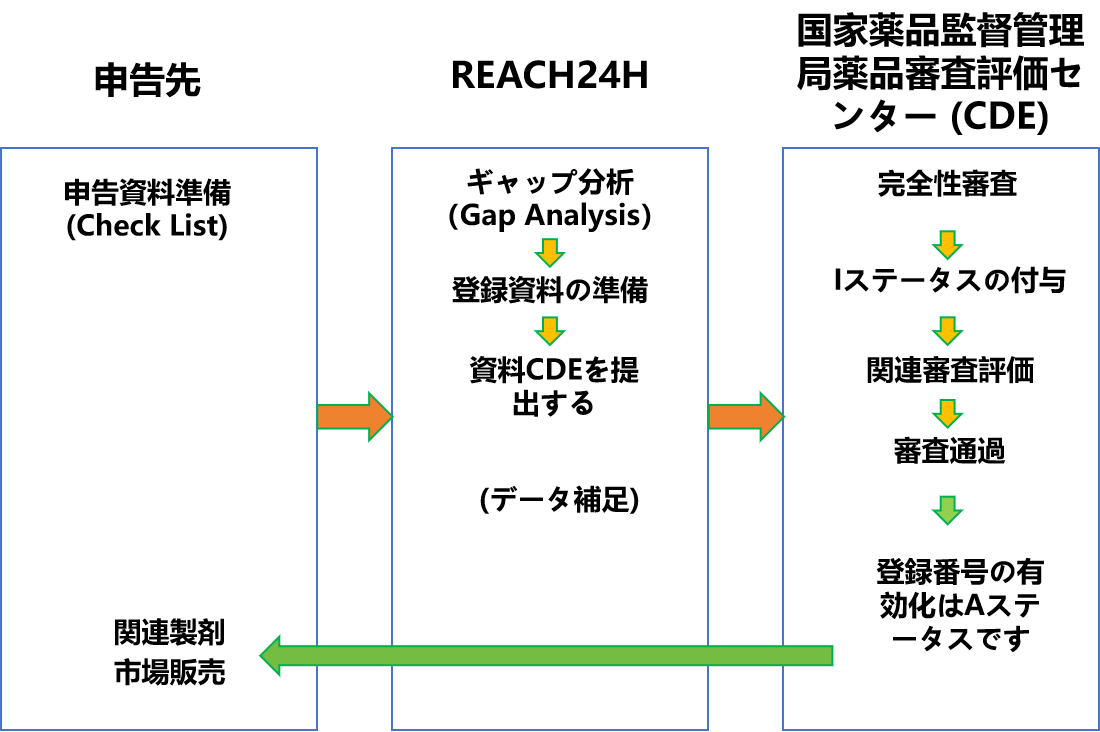
医薬品包装材料登録の流れ図
医薬品包装材料の登録手順
· CDEポータルに医薬品包装材料の基本情報を記入し、CD-ROMの形でCDEに登録資料を提出します。
· CDEは、情報を受け取ってから5営業日以内に登録情報の完全性レビューを実施するものとします。
· 情報が不完全な場合、医薬品包装材料企業は、要件を満たすまで登録情報を補足する必要があります。 CDEは、関連する登録情報を公表し、Iステータス登録番号(登録番号構成:B+4桁の年番号+7桁のシリアル番号)を付与します。
· 梱包材が協会の審査に合格すると、登録番号はAステータスに有効化されます。
医薬品包装材料の登録情報
医薬品協会の審査、承認、監督に関連する関連事項のさらなる改善に関する国家食品薬品監督の発表(2019年第56号)は、医薬品包装材料をその用途に応じて次のカテゴリに分類しています。
· 国内外の医薬品に使用されていない医薬品包装材料(新素材、新構造など)
· 国内および海外で販売されている医薬品に使用されてきたが、薬物投与の経路を変更し、リスクを増加させた医薬品包装材料。
· 国内および海外で販売されている医薬品には使用されていないが、食品と直接接触する食品包装に使用されていることを証明できる医薬品包装材料(経口製剤のみ)。
· 同じ投与経路で市販された医薬品に使用された医薬品包装材料。
 · その他
· その他
提供される登録要件は、薬物の使用または曝露のリスクによって異なります。 これには、次の内容が含まれます。注:同じ製造プロセスと材料、同じ機能を持つ製品は、同じ医薬品包装材料として登録でき、医薬品包装材料企業は同じ登録番号で生産モデルと仕様を登録できます。
私達の利点
· 規制研究および包装材料の登録と宣言における13年以上の経験。
· 正常に宣言された医薬品包装材料には、ガラス輸液ボトル、プラスチック輸液ボトル、粉末液ダブルチャンバーバッグ、液体マルチチャンバーバッグ、コンビネーションキャップ、ゴム栓、イソプレンガスケット、プレフィルドシリンジ、注射バイアル、経口液体ペットボトル、経口固体プラスチックボトル、経口固体複合フィルム、プラスチックアンプル、ガラスアンプルなどがあります。

