概要
手指消毒剤は、人間の手で使用する抗菌製品として、米国では市販(OTC)局の消毒剤カテゴリに分類され、食品医薬品局(FDA)によって規制管轄されています。コンプライアンス要件は、環境保護庁(EPA)によって規制されている環境消毒剤とは大きく異なります。主な規制はFFDCA(連邦食品医薬品化粧品法)です。
一般的に、米国で市販薬を販売するには2つの方法があります。
· FDAの承認申請を提出する必要がある新薬申請(NDA)後の承認済み新薬販売。
· OTCモノグラフによるOTC販売。
OTC医薬品モノグラフは、許容される成分、用量、製剤、およびラベルを網羅した一種の「レシピブック」です。OTCモノグラフで販売されているOTCダグにはFDAの事前承認は必要ありません。
手指消毒剤の場合、企業はOTCモノグラフの要件に従って製品を製造し、FDAの事前承認なしに製品を直接米国市場に投入できます。
手指消毒剤の許認可に必要なコンプライアンス要件または注意事項
登録範囲
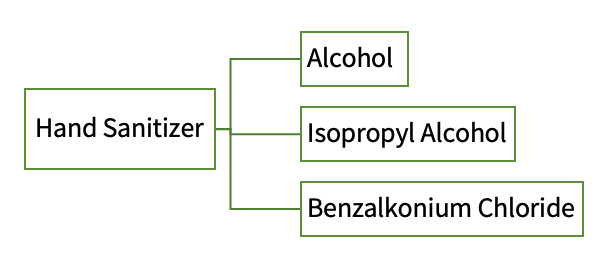
手指消毒剤については、現在、アルコール(エタノール)、イソプロピルアルコール、塩化ベンザルコニウムの3つの有効成分のみがOTCモノグラフの非承認経路を通じて入手可能です。
商品の要件
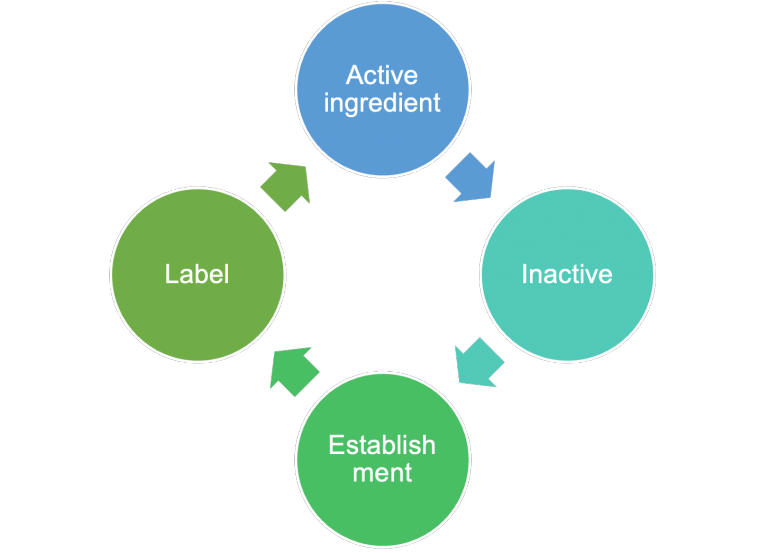
1. 手指消毒剤のOTCモノグラフでは、有効成分がアルコール、イソプロピルアルコール、塩化ベンザルコニウムである必要があります。内容物は、特定の要件も満たしている必要があります:少なくとも60%のエタノールを含むアルコールベースの手指消毒剤。少なくとも70%のエタノールを含むイソプロピルアルコールベースの手指消毒剤。
2. 不活性成分は、FDAの不活性成分データベースにある物質を使用する必要があります。
3. 製造施設は、現在の適正製造基準(cGMP)の要件を満たす必要があります。
4. 手指消毒剤のラベルは、対応するラベル表示規則に準拠している必要があります。
コンプライアンス義務
手指消毒剤がOTCモノグラフの要件を満たしていることを前提に、手指消毒剤を市場に投入する前に、以下のコンプライアンス作業を行う必要があります。
1. 関連するメーカーとトレーダーのDUNS番号申請。
2. FDAに製造施設の登録。
3. 対象製品のNational Drug Number(NDC)の申請。
4. FDAへの製品リスト提出。
5. 製造施設と製品情報の年次更新。
米国外の企業の場合、米国内の代理店を通して、上記5つのコンプライアンス要件を履行する必要があります。
登録対象者
手指消毒剤のメーカーに加えて、川下の貿易業者、輸入業者、流通業者もFDAに製品を出品することができます。
REACH24Hのサービス内容
· FDA設立登録代行
· NDCアプリケーション
· 手指消毒剤ラベルの見直し・作成代行
· 手指消毒剤のリスト提出
· 手指消毒剤の年次更新と再登録(REACH24H USA支社が米国内にて対応)
REACH24Hの利点
· 豊富な経験:FDAの手指消毒剤規制を長年にわたって法規制と市場動向を常に把握できています。
· 優れたパフォーマンス: 2023 年 12 月までに、REACH 24H は 100% の合格率でを維持し、申請代行業務を履行しております。
· 強力な技術力:分析化学、化学工学、生物学、薬理学、環境、その他の専門的背景を持つ強力な技術チームで構成される技術力にてサポートします。
· 強い言語力によるグローバル対応:カスタマーサービススタッフが英語、中国語、日本語、イタリヤ語、ドイツ語、その他の言語能力を有し、顧客様の海外進出に効率よく・スピーディーな対応を展開可能です。
· 豊富な経験蓄積:農薬および消毒剤の規制対応と技術コンサルティング業務が本事業部のコア業務として長年従事し、豊富な経験を蓄積できサービス構成ができておりお客様のニーズによってぴったりなサービスを創出・提案することが可能です。
· 優れたソリューション:国内外の多くの優れた研究所・試験室と協力し、企業向けの専門的で効率的なテストプログラムを設計し、質の高いサービスを提供いたします。
良好な関係規制:当局担当者や専門家、協会組織との長期的な友好的なコミュニケーションチャネルを確立し、サービスの品質と効率を大幅に向上させることが可能です。

