欧盟农药法规:欧盟PPP-植物保护产品法规
欧盟农药法规Regulation (EC) No 1107/2009(以下简称欧盟PPP法规)于2009年颁布以取代旧法令Directive 91/414/EEC,并于2011年6月14日起正式实施,是目前欧盟层面农药管理最重要的法规。
与此配套的,Regulation (EU) 283/2013和Commission Regulation (EU) 284/2013分别规定了欧盟农药活性物质和制剂产品登记的数据要求。此外,还有一系列欧盟委员会EC、欧盟食品安全局EFSA和各个成员国颁布的指南文件,作为对欧盟PPP法规的细化和补充,详细阐述具体登记操作细节问题(如登记流程、评审费用、文献检索、数据保护、风险评估等)。
主要的监管机构有欧盟委员会(European Commission, EC)欧洲食品安全局(European Food Safety Authority, EFSA),以及各成员国主管当局(Competent authorities of MS)。
企业义务及应对策略
登记范围
欧盟PPP法规的监管范围包括农药活性物质、安全剂、增效剂、农药制剂、辅助剂(如桶混助剂)等。
根据欧盟PPP法规,农药产品在欧盟的登记分为两个层面:
一是欧盟层面的活性物质批准(原药登记)
二是成员国层面的制剂产品授权(制剂登记)
 登记主体
登记主体
欧盟境内外的农药生产商、贸易商等。
登记流程
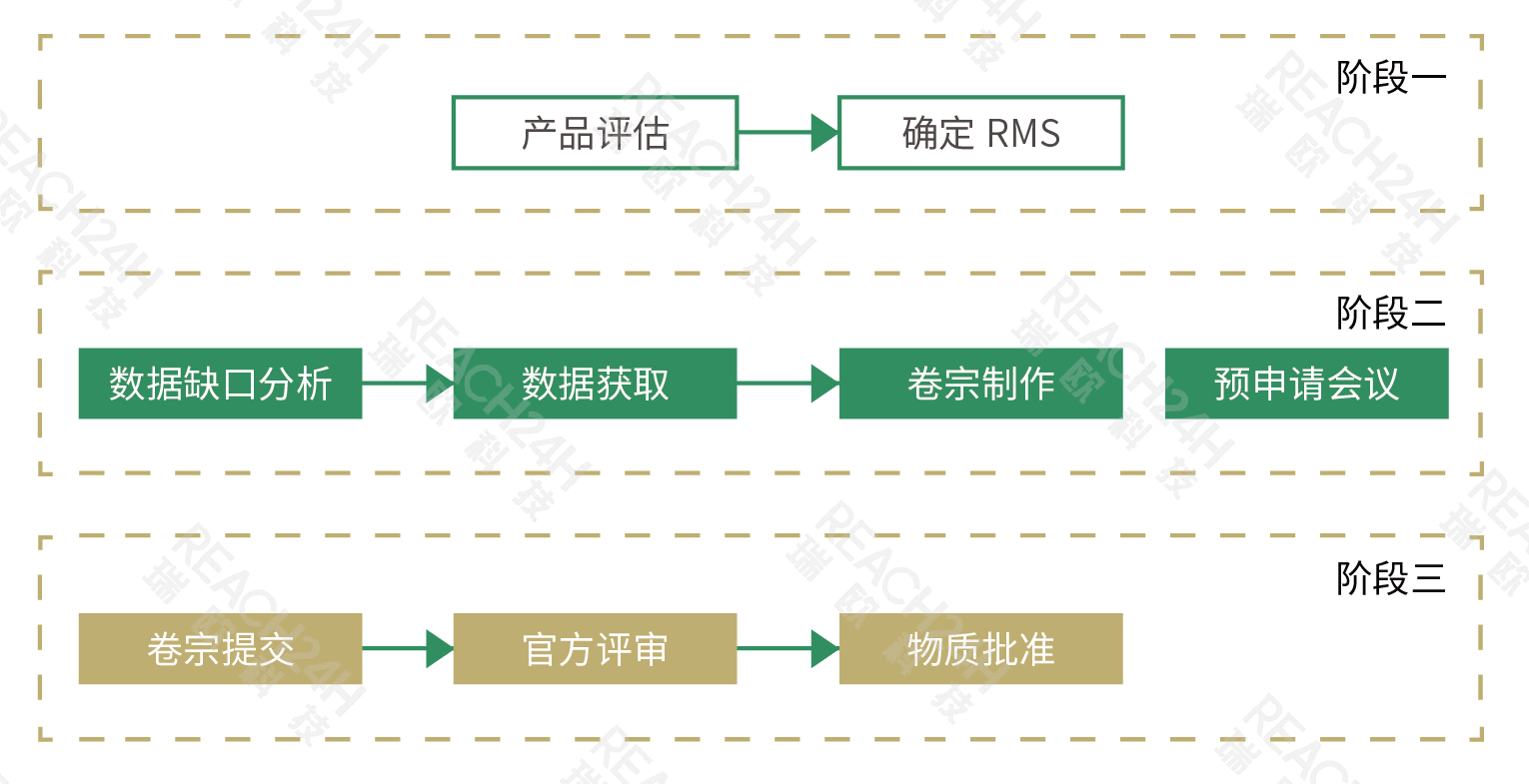
欧盟农药活性物质批准评审流程
一般来说,对于一个新的农药活性物质,欧盟层面统一评审一次,评审流程如下图所示:企业需要先选定评估成员国(RMS)提交申请一套完整的卷宗,由评估成员国进行评估并出具评估报告草案;评估报告草案完成后,会发给EFSA、欧盟委员会及欧盟其他成员国,并由EFSA组织进行评估草案的公开评议;所有成员国达成一致意见后,评估结果即可通过。所以物质一旦批准生效,整个欧盟层面都会认可,而批准后的物质来源,就会成为原药参考来源,享有10年批准有效期。
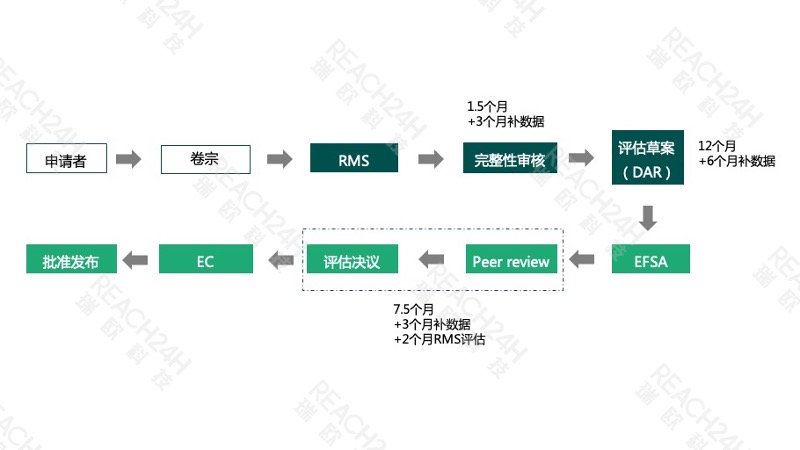
欧盟原药等同性评估(欧盟TE评估)
除了原药参考来源,其他非专利原药进入欧盟市场需要与欧盟批准的参考来源进行等同性 (Technical Equivalence, TE ) 评估,欧盟TE评估通过之后在欧盟层面有效,可以进入整个欧盟市场。
一般有如下三种不同的情况需进行欧盟TE评估:
新原药来源为参考来源生产商以外的生产商生产
原参考来源或TE批准来源由小试或中试变成大规模生产
原参考来源或TE批准来源改变了生产工艺或生产厂址
产品授权
制剂产品授权是成员国层面的,产品销售需要获得所有目标国家的授权许可。
为了减少重复的评审工作,缩短产品投放欧盟市场的时间,欧盟PPP法规引入区域评估系统,对产品登记采用区域评审制度。根据区域评估的相关规定,欧盟地区按照农业气候条件划分为北、中、南3个区域,实行核心卷宗区域统一评估。除核心卷宗外,相关成员国可以有本国额外的数据要求(如药效、残留、环境归趋等),与本国农业环境条件相关的附加数据包含在成员国卷宗中,由各个成员国单独评审。对于施用不受农业气候条件影响的农药产品,比如室内用途(采后处理、温室、仓库)和种子处理的农药产品,其制剂登记时,将整个欧盟视为一个区域进行评估。
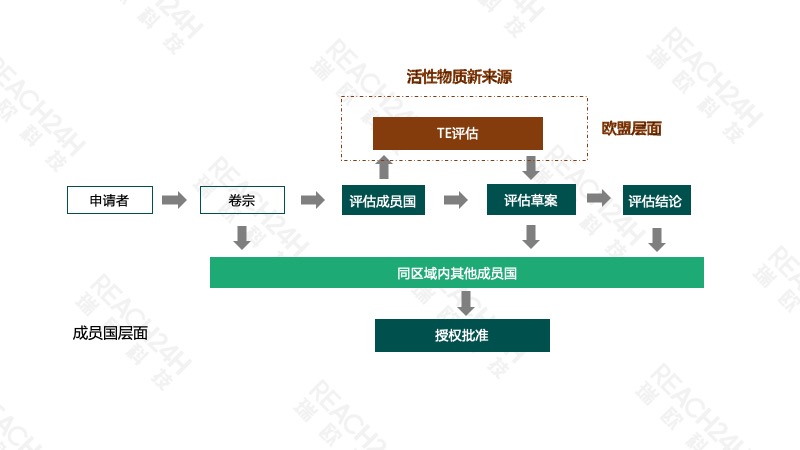
企业申请区域授权具体流程如下图。申请制剂登记时,产品所用的原药来源必须是参考来源或者与参考来源等同的新来源(TE来源)。另外,在产品授权评估过程中,产品的卷宗、评估草案及评估决定除RMS以外,还会发送给同区域内其他所有成员国,并接受这些成员国的评议意见。由此,通过一个成员国的产品授权后,产品出口相同区域内的其他成员国就可以申请区域互认,这样大大简化了产品授权的周期和成本。
评估成员国(RMS)选择
申请原药TE评估或制剂产品授权时,需要选择一个主评估国(RMS),RMS选择的主要考虑因素如下
欧盟农药再评审
欧盟PPP法规下,活性物质首次批准以后一般享有10年的有效期(不包括低风险农药和候选替代物质),在活性物质有效期到期前3年,企业需提交物质再评审申请。
产品登记的有效期与活性物质批准状态相关,只要活性物质处于批准状态,产品登记就一直有效。活性物质再评审通过之后,相应的产品也要进行续展登记。
欧盟农药登记数据保护
为了保证登记申请人的权益,欧盟对用于农药登记的数据会进行保护。数据保护一般以制剂产品授权批准之日开始算,一般情况下,产品首次批准数据 (包括原药批准和制剂授权数据)享有10年的有效期(低风险农药13年),再评审数据享有30个月的有效期。
我们的服务
欧盟原药等同性评估(欧盟TE)
欧盟农药新活性成分登记
活性物质再评审申请
欧盟农药制剂产品授权(Article 33&34 登记)
Data Matching评估
QSAR 报告
内分泌干扰风险评估
产品合规分析/数据缺口分析报告
数据评估/缺口分析/豁免分析/专利分析
GLP实验代理和监理
法规综合咨询和定制化培训服务
欧盟分公司设立
欧盟PPP农药登记项目经验
在欧盟农药登记方面,我们是国内最早开始研究原药等同性评估并成功取得批准信的机构之一,且列入欧盟农药登记CADDY卷宗编写服务供应商。截止目前,瑞欧已经成功帮助企业完成近200个欧盟TE申请,涉及产品达100多个。经过10多年合规经验,团队已拥有非常丰富且成熟的官方渠道资源,目前已经在欧盟十几个国家递交过申请并顺利取得通过。
此外,英国/荷兰/法国/意大利/比利时/德国/波兰/奥地利/捷克/爱尔兰等政府官方与我们保持着良好的合作关系,其中英国和荷兰等国家官方代表曾连续多年作为演讲嘉宾出席瑞欧科技主办的全球化学品法规峰会。
我们的优势
扎实的专业技术能力
10多年欧盟农药管理法规合规实践硕果累累,具备独立自主完成欧盟农药登记项目服务能力。
丰富的成功项目经验
瑞欧已成功帮助国内外企业完成数百个欧盟PPP申请,涉及产品达100多个。其中,在Top100强的中国农药企业中,合作企业数量高达80%。
合理透明的收费标准
切实考虑中国企业实际情况,提前告知收费标准,按照项目打包收费,费用合理、透明。合理化的项目分阶段区分收费模式,减少非必要成本支出。
用“心”做事,以“专业”服人
瑞欧不仅擅长根据自身多年经验以及扎实的技术功底,最大程度协助企业充分完善登记资料,提高资料质量和可靠性;还善于运用技术专业为企业与国外农药评审机构进行辩护,帮助企业豁免部分资料要求,降低企业的登记费用和周期成本。
欧盟官方关系及语言沟通优势
瑞欧在爱尔兰设立了子公司,与欧盟EFSA、英国HSE、荷兰Ctgb等欧盟官方及专家建立了长期友好的沟通合作关系,可帮助企业定制优质高效的项目方案,提高登记项目服务质量和效率。
瑞欧中国总部可为中国企业提供无时差,无障碍语言沟通优势,服务质量及效率更有保障。爱尔兰子公司能为欧盟登记项目的申请提供坚实的技术保障和官方维系渠道优势。







 化学品
化学品
 食品接触材料
食品接触材料
 化妆品
化妆品
 绿色双碳
绿色双碳