法规概述
根据《食品安全法》规定,使用保健食品原料目录以外原料的保健食品和首次进口的保健食品应当经国务院食品安全监督管理部门注册;
首次进口的保健食品中属于补充维生素、矿物质等营养物质的,应当报国务院食品安全监督管理部门备案;
其他保健食品应当报省、自治区、直辖市人民政府食品安全监督管理部门备案。
自2017年5月1日起,对使用列入《保健食品原料目录》的原料生产和进口保健食品的,国内生产企业和境外生产厂商应当按照《保健食品注册与备案管理办法》及相关规定进行备案。
主管部门
国家市场监督管理总局(SAMR)
相关法规
《保健食品注册与备案管理办法》
《辅酶Q10等五种保健食品原料备案产品剂型及技术要求》
《保健食品原料目录 营养素补充剂(2020年版)》
《保健食品及其原料安全性毒理学检验与评价技术指导原则(2020年版)》
《保健食品原料用菌种安全性检验与评价技术指导原则(2020年版)》
《保健食品理化及卫生指标检验与评价技术指导原则(2020年版)》
进口流程
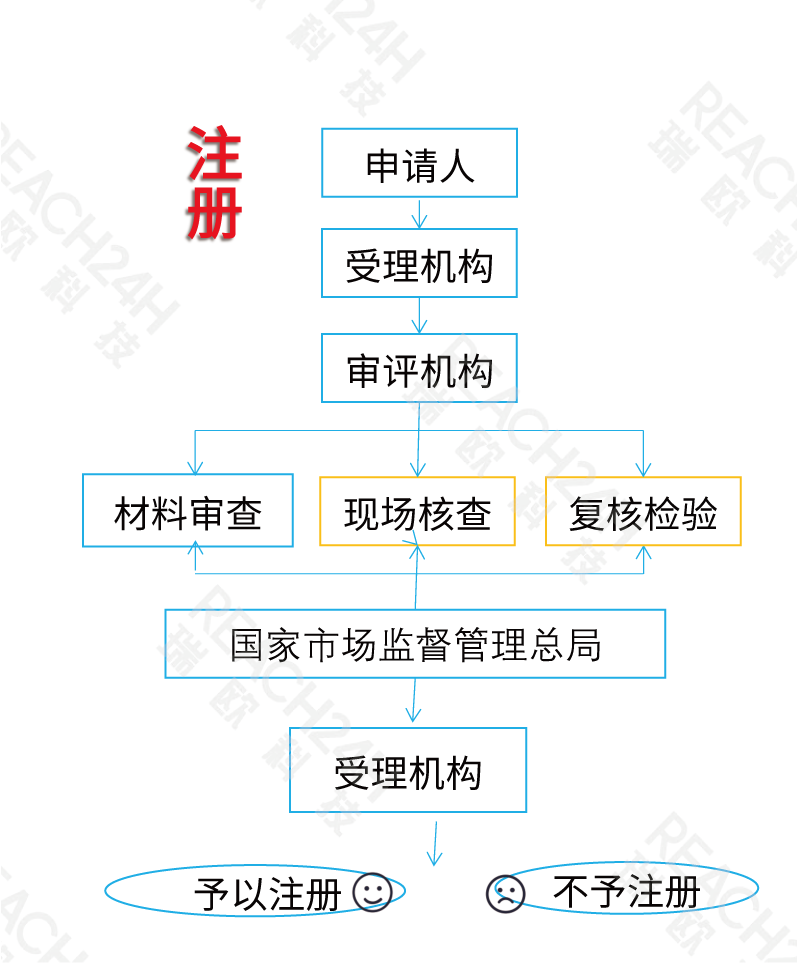
注册
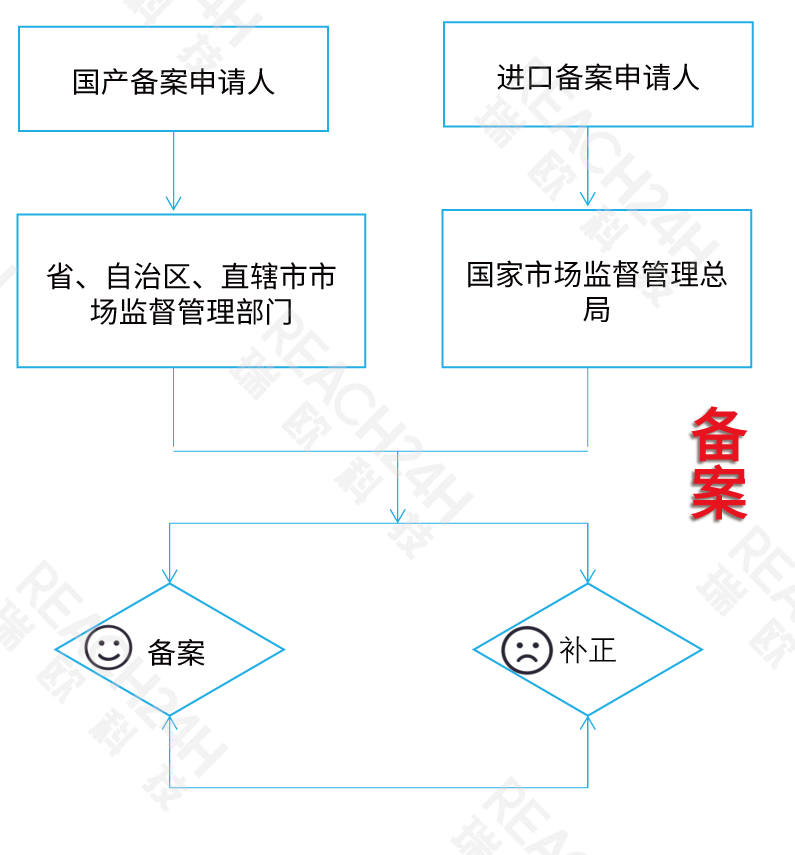
 备案
备案
我们的服务
法规咨询
形式:网络、电话、面对面
主要内容:
保健食品管理法规解读
保健食品注册与备案流程
保健食品注册与备案策略分析
产品研发咨询
国产保健食品备案
目的:获得国产保健食品的上市许可
主要内容:
备案可行性研究
备案材料准备
备案材料专家审核
提交备案、取得备案号
进口营养素补充剂备案
目的:获得进口营养素补充剂的上市许可
主要内容:
备案可行性研究
备案材料准备
备案材料专家审核
提交备案、取得备案号
保健食品注册(国产/进口)
目的:获得需注册保健食品上市官方许可
主要内容:
注册预评估:可行性、周期、费用
注册卷宗制作
注册测试监理
专家、评审部门沟通





 化学品
化学品
 食品接触材料
食品接触材料
 化妆品
化妆品
 绿色双碳
绿色双碳
 境外农药登记
境外农药登记
 中国农药登记
中国农药登记