法规概述
特殊医学用途配方食品,是指为满足进食受限、消化吸收障碍、代谢紊乱或者特定疾病状态人群对营养素或者膳食的特殊需要,专门加工配制而成的配方食品,包括适用于0月龄至12月龄的特殊医学用途婴儿配方食品和适用于1岁以上人群的特殊医学用途配方食品。
法规要求
根据《食品安全法》,特殊医学用途配方食品应当经国务院食品药品监督管理部门注册。注册时,应当提交产品配方、生产工艺、标签、说明书以及表明产品安全性、营养充足性和特殊医学用途临床效果的材料。
自2019年1月1日起,在我国境内生产或向我国境内出口的特殊医学用途配方食品应当依法取得特殊医学用途配方食品注册证书。
主管部门
国家市场监督管理总局(SAMR)
相关法规
《特殊医学用途配方食品注册管理办法》
《特殊医学用途配方食品标签、说明书样稿要求(试行)》
《特殊医学用途配方食品稳定性研究要求(试行)》
《特殊医学用途配方食品注册申请材料项目与要求(试行)》
《特殊医学用途配方食品注册生产企业现场核查要点及判断原则(试行)》
《特殊医学用途配方食品临床试验质量管理规范(试行)》
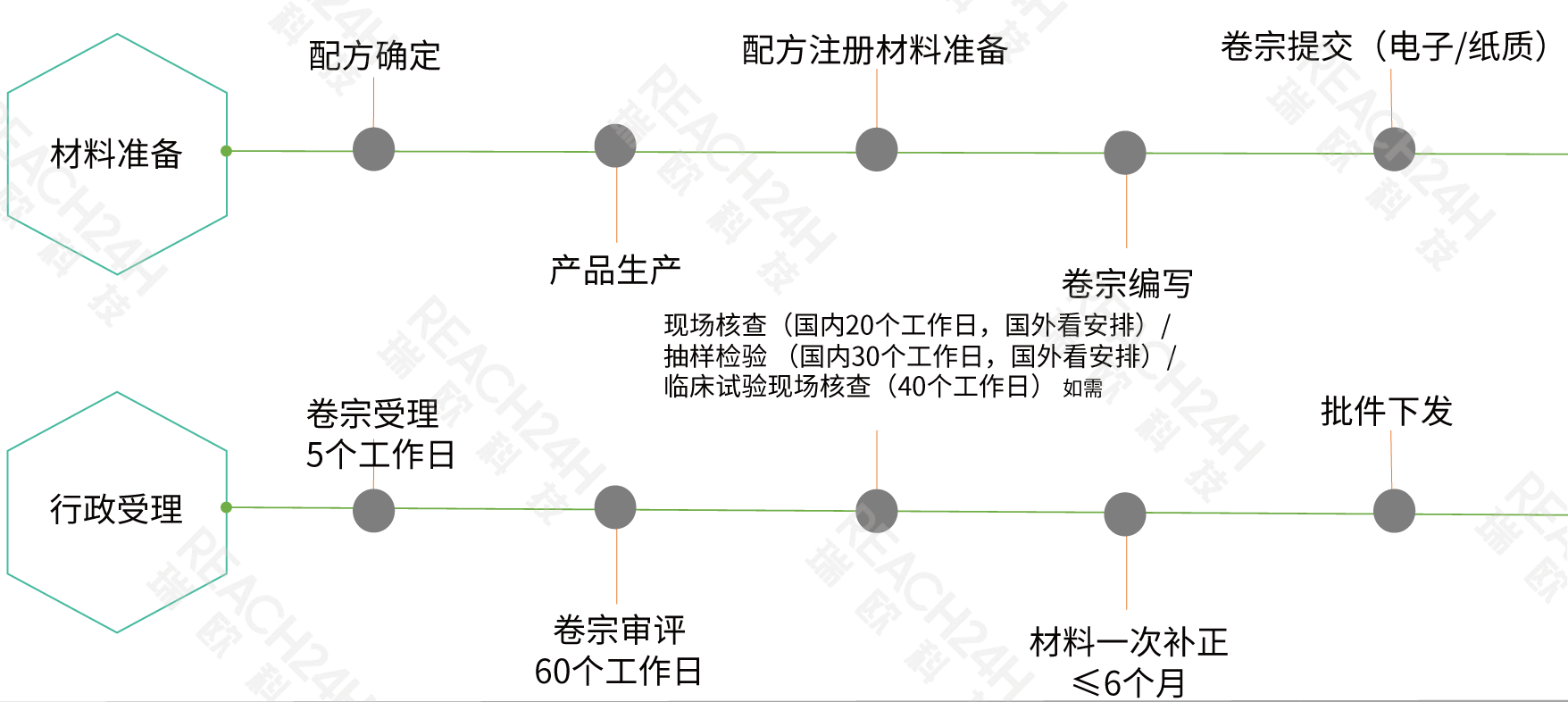
进口流程
我们的服务
法规咨询
形式:网络、电话、面对面
主要内容
特殊医学用途配方食品管理法规
特殊医学用途配方食品注册流程
特殊医学用途配方食品注册策略分析
针对产品定制化的注册咨询和培训
产品合规审核
目的:确定特医产品是否符合中国的质量规格要求
主要内容
产品配方审核
产品标签审核
原辅料合规审核
产品研发咨询
产品注册预评估
目的:评价生产企业是否具有完善的研发、检测、生产能力
主要内容
审核生产企业的资质
审核产品研发资料
生产工厂现场审核
与主管部门、权威专家沟通
特殊医学用途配方食品注册
目的:取得需注册特殊医学用途配方食品的上市许可
主要内容
注册预评估:可行性、周期、费用
注册卷宗制作
注册测试监理
专家、评审部门沟通





 化学品
化学品
 食品接触材料
食品接触材料
 化妆品
化妆品
 绿色双碳
绿色双碳
 境外农药登记
境外农药登记
 中国农药登记
中国农药登记